
【通用名】达伐吡啶/氨吡啶
【适应症】多发性硬化MS
【上市情况】2010 (FDA)、2021.4(NMPA)目前在全球数十个国家上市
【原研公司】Biogen(渤健)
【剂型】缓释片
【专利情况】化合物专利已过期
【注册分类】新4类
【医保】国家医保乙类
1. 发病率及患病率上升:多发性硬化(MS)在我国属于罕见病,发病率约为5/100 000,全国发病人数约7万人,近年来MS发病率及患病率呈上升趋势。
2. 用药率及复购率高:MS 是一种以中枢神经系统炎性脱髓鞘病变为主要特点的疾病,如得不到及时的规范治疗,大多数患者会因不可逆的神经功能缺损而致残。MS常见症状包括视力下降、复视、肢体感觉障碍、肢体运动障碍、共济失调、膀胱或直肠功能障碍等,对生活质量影响大,患者用药率高;MS目前无法治愈,患者需要终身服药,市场规模不容忽视。
3. 国家罕见病政策提升商业化速度:国内政策大力支持罕见病研发及生产,在评审、市场准入、医保等环节均设立绿色通道,商业化速度提升。多发性硬化(MS)是我国首批罕见病目录品种,原研产品被列入临床急需用药目录,通过快速通道获批上市。
4. 达伐吡啶/氨吡啶目前唯一被美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)批准针对于改善MS患者步行能力的药物。它与疾病修正治疗(DMT)药物联合使用,提供了短期改善步行能力,长期减少疾病致残的综合治疗方案。行走障碍是最具破坏性的功能障碍,几乎所有的MS患者最终会经历不同程度的行走障碍。
1. 达伐吡啶市场:
全球市场全球多发性硬化症治疗药物市场预期将由2020年的234 亿美元增长到2025 年的257 亿美元,2020 年至 2025 年复合年增长率为1.9%。
2016至2018年达伐吡啶全球平均销售额约6亿美元,中国市场尚处于起步阶段。
2. 注册情况:
制剂:1家上市,1家在评审
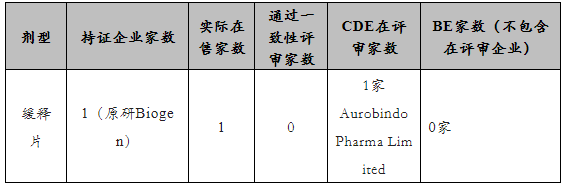
API:原辅包平台备案数量:1家进口,0家国产
参考: