
随着EPIC-PEP和EPIC-SR研究结果未达预期,Paxlovid对于一般风险人群及暴露人群的治疗尝试宣告失败,而随着疫苗接种率大幅提升,该人群已成为目前最主流的目标用药人群。Paxlovid真的走到穷途末路了吗?今天我们就Paxlovid临床试验、获批适应症进行详细分析。
1.辉瑞Paxlovid开展主要III期临床试验(文献1-3)
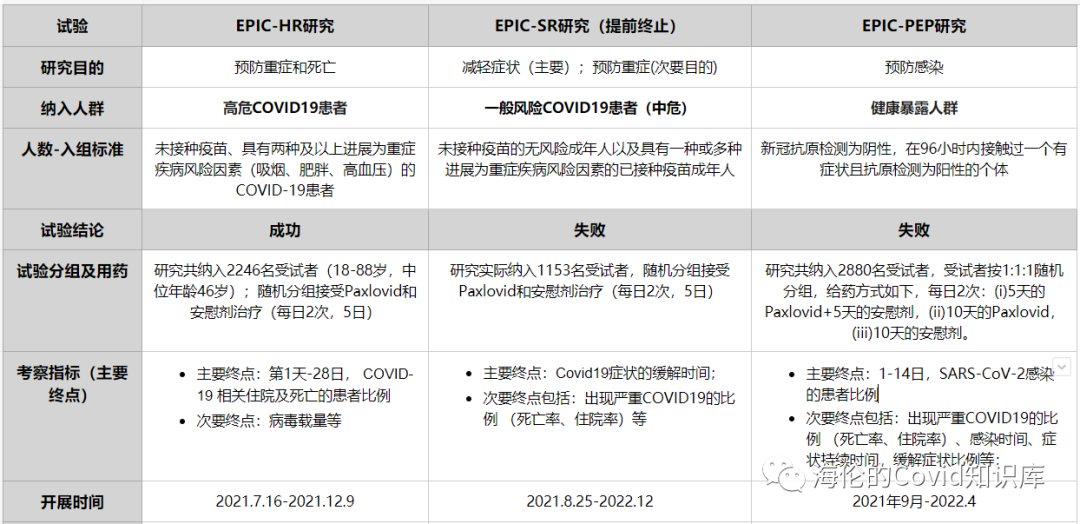

2.进展为重度COVID-19的风险因素包括哪些?(文献4-5)
EPIC-HR研究中的高风险入组人群是指:吸烟、肥胖、高血压
美国CDC定义的可能进展为重度COVID-19的风险因素包括:
年龄:65岁以上;
种族和民族
临床证据证实的风险因素:
证实的高风险:哮喘、肿瘤、脑血管病、慢性肾病、慢性肺病、慢性肝病、糖尿病、心脏病、艾滋病、怀孕、免疫缺陷、吸烟等等
潜在的高风险(无系统综述或尚未完成CDC系统综述程序):超重、地中海贫血等。
混合证据(有系统综述或已完成CDC系统综述程序):高血压、乙肝/丙肝等。
3.目前辉瑞EUA授权适应症是什么?(文献6-7)
美国:轻度至中度成人和儿科患者(12岁及以上体重至少40公斤),SARS-CoV-2病毒检测结果呈阳性且具有进展为严重COVID19(住院或死亡)的高风险因素
中国:适应症为发病5天以内的轻型和普通型且伴有进展为重症高风险因素的成人。
4.除了上述适应症,Paxlovid还有什么市场机会?(文献8-9)
从目前信息看,有两个方向可以拓展:
延长治疗周期:由于目前Paxlovid存在复阳现象,科学界有一个推测是Paxlovid“过于有效”,能在人体免疫系统警报被触发前,消灭大部分新冠病毒,但有一小部分病毒存活下来。一旦用药结束,在那些没有形成特异性免疫的患者体内,幸存病毒或能重新繁殖,基于该推论,或应增加药物疗程,比如从5天增至8或10天。由于出现反弹时,患者大多完成药物治疗、结束隔离状态。这可能造成病毒新一轮传播。2022年5月18日,美国国家过敏症和传染病研究所所长安东尼・福奇表示NIH(美国国立卫生研究院)正与辉瑞进行协商,研究是否需要延长治疗周期预防再感染(复阳)。截止2022年6月19日,clinicaltrials.gov上尚无该类临床试验登记。
拓展新适应症(新冠后遗症):路透社报导两名患者在服用辉瑞的抗病毒药Paxlovid后,long COVID(新冠感染后3个月的遗留症状),包括慢性疲劳、头痛和睡眠障碍有所缓解或完全消失。科学家们推断Paxlovid 可能只对那些由于病毒残留而出现长期症状的患者有益。其他病人的症状可能是由于慢性炎症或自身免疫问题而不太可能受益。耶鲁大学长期从事冠状病毒疾病研究的Akiko Iwasaki表示: “研究目标不是治愈所有人,而是了解谁能从中受益。即使只有10% 的患者有积极的反应,这仍然意味着如果帕洛韦或其他治疗方法有效,数百万人的冠状病毒疾病症状会得到改善。”截止2022年6月19日,clinicaltrials.gov上尚无该类临床试验登记。
编者浅见
1.从Paxlovid试验入组标准及统计学分析结果可看出,与安慰剂相比,Paxlovid仅对“未接种疫苗、具有两种及以上进展为重症疾病风险因素(吸烟、肥胖、高血压)”的患者有统计学差异,而在其他人群中,无统计学意义。由于目前全球发达国家及部分发展中国家的疫苗接种率非常高,如果按照该定义,Paxlovid的适用范围被大大限制。
2.从EUA授权使用的适应症可以看出:PAXLOVID能用于治疗轻度至中度成人和儿科患者(12岁及以上体重至少40公斤),SARS-CoV-2病毒检测结果呈阳性且具有进展为严重COVID19(住院或死亡)的高风险因素“,和临床试验相比较,该适用范围大幅增加。
在CDC发布的“可能进展为重度COVID-19的风险因素列表”中,风险因素包含年龄、种族、多种临床证实的高风险(包括各类疾病),远超过辉瑞临床试验中的吸烟、肥胖、高血压。
在EUA及上述风险列表中,均未提及“患者的疫苗接种状态”。
3.综上所述,虽然从临床试验结论看,现阶段Paxlovid适用人群范围很窄,但从授权使用的适应症看,由于对于“风险因素”定义的差异(尤其是未定义患者疫苗接种的状态),Paxlovid的适用范围被极大拓展了。另外,辉瑞未来还可以通过延长治疗周期和拓展新冠后遗症来扩大使用范围及数量。作为已被证实的目前全球最有效的新冠抗病毒小分子,Paxlovid还有很大的拓展空间,并未走到穷途末路的境地。
4.辉瑞Paxlovid处于EUA状态,尚未正式批准,FDA在正式批准Paxlovid时,是否会考虑EPIC-SR研究的结果,我们将持续关注。
参考阅读
https://www.clinicaltrials.gov/ct2/show/NCT05047601?term=EPIC-PEP&draw=2&rank=1
https://www.clinicaltrials.gov/ct2/show/NCT04960202?term=EPIC-HR&draw=2&rank=1
https://www.clinicaltrials.gov/ct2/show/record/NCT05011513?term=EPIC-SR&draw=2&rank=1
https://www.clinicaltrials.gov/ct2/show/NCT04960202?term=EPIC-HR&draw=2&rank=1
https://www.cdc.gov/coronavirus/2019-ncov/hcp/clinical-care/underlyingconditions.html
https://aspr.hhs.gov/COVID-19/Therapeutics/Products/Paxlovid/Pages/emergency-use-authorization.aspx
关于调整抗新型冠状病毒药物PF-07321332/利托那韦片(Paxlovid)适应症等内容的通知 国卫办医函〔2022〕81号
https://www.usnews.com/news/top-news/articles/2022-05-18/u-s-to-study-whether-longer-paxlovid-course-needed-to-combat-reinfections
https://www.advisory.com/daily-briefing/2022/05/12/paxlovid-long-covid