
导读
新冠大流行期间,在不到一年的时间内开发了多种疫苗,其中一些使用了以前在疫苗生产中没有使用过的技术,这意味着短期和长期不良反应的经验,包括过敏反应的风险,是非常有限的。为了更好地了解2019冠状病毒疾病疫苗过敏反应的管理和机制,并使更多有过敏史的人接种疫苗。欧洲药物过敏网(ENDA,European Network on Drug Allergy)和欧洲变应性反应与临床免疫学会(EAACI,European Academy of Allergy and Clinical Immunology)根据文献调查和分析的结果,2022年2月发布了《Allergies and COVID-19 vaccines: An ENDA/EAACI Position paper》,对有过敏史的患者如何接种疫苗提出了详细的建议。
指南观点
1.如何对患者进行过敏的判定和处理?
根据患者的过敏史进行风险分级(如下图),建议对有以下病史的人进行过敏评估: 1对含有聚乙二醇或衍生物的注射药物或疫苗过敏; 2对含有口服/局部聚乙二醇的产品过敏; 3不明原因的反复过敏; 4怀疑或确认对任何 mRNA 疫苗过敏; 5确认对聚乙二醇或衍生物过敏。
对于需要进行过敏测试的患者,进行点刺试验(Prick tests)来判定是否过敏(用待测试的疫苗、疫苗-PEG 4000或PEG 3000水溶液(如果无法获得,使用含有PEG的结肠镜检查制剂)-PEG 2000水溶液(50%)-聚山梨酯80水溶液(20%)进行点刺试验)
根据点刺试验结果来判定疫苗使用:在皮试阴性的情况下:可以通过1小时监测进行疫苗接种。在使用一种辅料进行皮试阳性的情况下:如果可能,可以讨论疫苗的皮内试验,改变疫苗平台和辅料。必须讨论疫苗或分次接种的禁忌症。

2.疫苗过敏发生率有多高?
疫苗的严重过敏反应罕见,2020年12月,辉瑞-BionTech 2019冠状病毒疾病 mRNA 疫苗接种后报告了首例过敏反应病例,但科学文献迄今没有报道过敏反应导致的死亡。据报道,辉瑞-BionTech 2019冠状病毒疾病疫苗接种后的过敏反应发生率为每百万剂11.1次,比其他疫苗高出约10倍。2019冠状病毒疾病疫苗过敏反应的发生率估计为每百万剂7.91例。
3.疫苗过敏是如何产生的?欧洲已上市疫苗中所使用的辅料
需要区分疫苗的过敏反应和疫苗本身的不良反应。疫苗的过敏反应可由疫苗本身或其辅料引起。欧洲疫苗所使用的主要辅料如下:
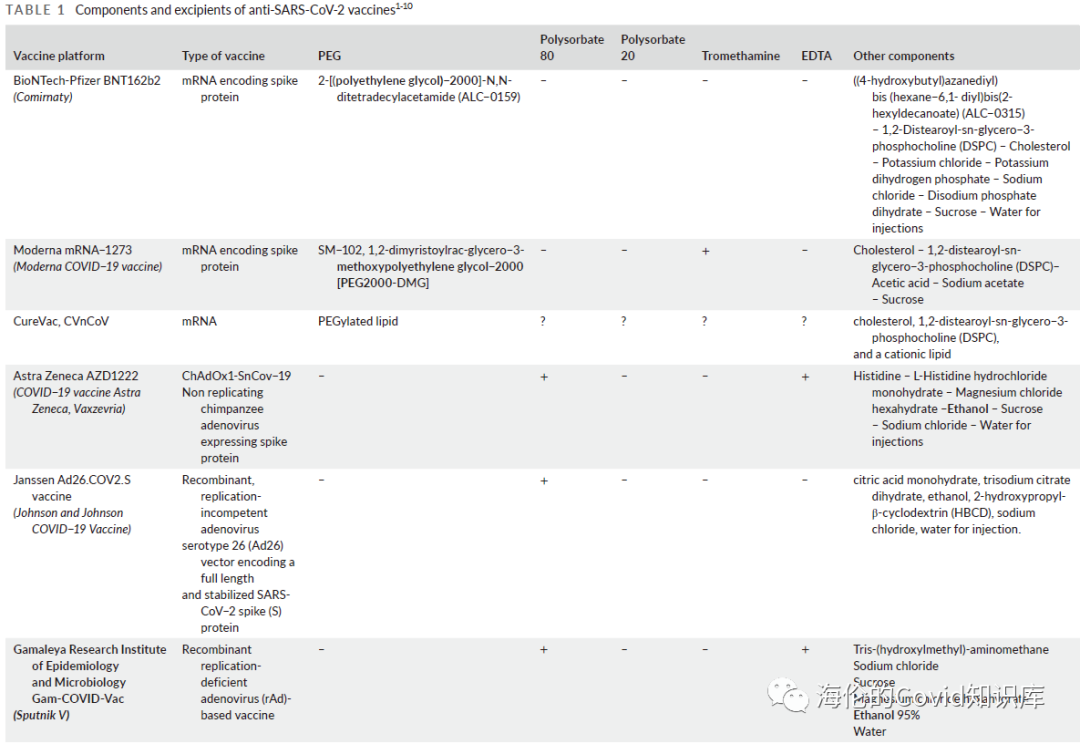

4.可能造成疫苗过敏的主要辅料?
Polyethylene glycol(聚乙二醇) :聚乙二醇,也称为 PEG 或凝胶E1521 ,是由聚合的环氧乙烷与水组成。聚乙二醇过敏可通过多种途径引发,包括口服、肌肉注射、关节内注射和静脉注射。
Polysorbates(聚山梨醇酯):PS80是一种非离子型亲水性聚乙氧基表面活性剂,又称 E433、吐温80、聚氧乙烯山梨醇单油酸酯。它是一种聚氧乙烯-山梨醇脂肪酸酯。
Disodium EDTA(EDTA二钠):乙二胺四乙酸二钠,一种氨基多羧酸,阿斯利康疫苗中使用。EDTA 盐作为防腐剂和稳定剂在食品、制造业、化妆品和医药领域有广泛的应用。化妆品及隐形眼镜护理药水曾引致接触性皮肤炎过敏。
Trometamol, tromethamine(曲美他莫,曲美他敏):用于防止尿酸和胱氨酸结石的形成,也用作药物辅料(非甾体抗炎药,CT 和 MRI 扫描的对比剂),在莫德纳mRNA 疫苗中使用。
5.试剂盒是否有机会?
嗜碱性粒细胞活化试验(BAT)被证明对于无法确定患者是否过敏,聚乙二醇酶联免疫吸附试验(ELISA)尚未标准化。目前还没有抗PEG 2000的IgE抗体(或IgM抗体),其被认为在触发补体介导的PEG超敏反应中发挥作用。有可能成为试剂盒开发的一个方向。
编者浅见
1.随着新冠大流行的爆发及持续,疫苗的接种未来有可能成为季节性防护的常态。有过敏史的患者对于疫苗过敏心存顾虑从而拒绝接种。
2.疫苗过敏主要由疫苗辅料造成,需要进行皮试来确定是否过敏,患者体验较差,而且医护操作较为繁琐,需要到专门的过敏门诊进行,很多国家或地区并不具备类似条件。如果开发体外试剂盒,可以配备到疫苗接种点,目前临床尚无可用的试剂盒,相关体外试剂盒的开发有可能成为未来的市场机会。
参考阅读
https://onlinelibrary.wiley.com/doi/10.1111/all.15241